ผู้เขียน:
Louise Ward
วันที่สร้าง:
11 กุมภาพันธ์ 2021
วันที่อัปเดต:
1 กรกฎาคม 2024
![🧪สารละลาย 3 : โมลาร์ | โมลต่อลิตร [Chemistry#15]](https://i.ytimg.com/vi/1_O7--9W08I/hqdefault.jpg)
เนื้อหา
ขนาดของอะตอมมีขนาดเล็กมากจนยากที่จะวัดเลขอะตอมของสารประกอบทางเคมีได้อย่างแม่นยำ เพื่อให้สามารถวัดปริมาณสารได้อย่างแม่นยำนักวิทยาศาสตร์จึงใช้หน่วยโมลแทนจำนวนอะตอมที่ระบุ หนึ่งโมลของสารถูกกำหนดให้เทียบเท่ากับจำนวนอะตอมของคาร์บอนที่มีอยู่ในไอโซโทปของคาร์บอน 12 กรัมซึ่งมีขนาดประมาณ 6,022 x 10 อะตอม ค่านี้เรียกว่าหมายเลข Avogadro หรือค่าคงที่ของ Avogadro สิ่งนี้เรียกอีกอย่างว่าจำนวนอะตอมใน 1 โมลของธาตุใด ๆ และ 1 โมลของมวลของสารเรียกว่ามวลโมลาร์ของสารนั้น
ขั้นตอน
วิธีที่ 1 จาก 2: คำนวณมวลโมลาร์ขององค์ประกอบ
ความหมายของมวลโมลาร์ มวลโมเลกุลของสารคือมวล (หน่วยเป็นกรัม) ของหนึ่งโมลของสารนั้น ในการคำนวณมวลโมลาร์ของธาตุให้คูณมวลอะตอมของมันด้วยปัจจัยการแปลงกรัมต่อโมล (g / mol)
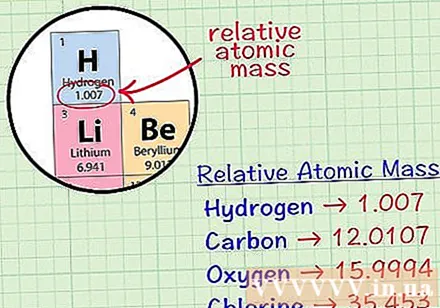
หาค่าเฉลี่ยของลูกบาศก์อะตอมของธาตุ อะตอมมวลเฉลี่ยของธาตุคือมวลเฉลี่ยในหน่วยอะตอมในตัวอย่างที่มีไอโซโทปทั้งหมดของธาตุนั้น ข้อมูลนี้มักได้รับในตารางธาตุ เมื่อค้นหาองค์ประกอบคุณจะพบอะตอมลูกบาศก์เฉลี่ยที่เขียนอยู่ด้านล่างสัญลักษณ์ทางเคมีขององค์ประกอบ ค่านี้ไม่ใช่จำนวนเต็ม แต่เป็นตัวเลขที่มีตำแหน่งทศนิยม- ตัวอย่างเช่นด้วยไฮโดรเจนอะตอมมวลเฉลี่ยคือ 1.007 ลูกบาศก์อะตอมเฉลี่ยของคาร์บอนเท่ากับ 12,0107; อะตอมมวลเฉลี่ยของออกซิเจนคือ 15,9994; คลอรีนมีมวลอะตอมเฉลี่ย 35,453

คูณอะตอมมวลเฉลี่ยด้วยค่าคงที่ของมวลโมลาร์ หน่วยของโมลาร์เหินกำหนดไว้ที่ 0.001 กิโลกรัมต่อโมลหรือ 1 กรัมต่อโมล ผลคูณของอะตอมมวลเฉลี่ยและค่าคงที่ของมวลโมลาร์จะแปลงหน่วยมวลอะตอมเป็นกรัมต่อโมลดังนั้นมวลโมลาร์ของไฮโดรเจนจะเท่ากับ 1.007 กรัมต่อโมลโดยคาร์บอนเท่ากับ 12 0107 กรัมต่อโมลออกซิเจน 15,9995 กรัมต่อโมลและคลอรีน 35,453 กรัมต่อโมล- องค์ประกอบบางอย่างมีอยู่ในธรรมชาติเป็นโมเลกุลที่ประกอบด้วยอะตอมเดียวกันตั้งแต่สองอะตอมขึ้นไป นั่นคือถ้าคุณต้องการคำนวณมวลโมลาร์ของสารประกอบที่ประกอบด้วยอะตอมมากกว่าหนึ่งอะตอมเช่นก๊าซไฮโดรเจนก๊าซออกซิเจนหรือก๊าซคลอรีนคุณต้องกำหนดมวลอะตอมเฉลี่ยของสารประกอบและคูณค่านี้ ด้วยค่าคงที่มวลโมลาร์ '' แล้ว '' คูณผลคูณที่คุณเพิ่งพบด้วย 2
- ด้วย H2: 1,007 x 2 = 2,014 กรัมต่อโมล; สำหรับ O2: 15,9994 x 2 = 31,9988 กรัมต่อโมล; และ Cl2: 35,453 x 2 = 70,096 กรัมต่อโมล
วิธีที่ 2 จาก 2: คำนวณมวลโมลาร์ของสารประกอบ

กำหนดสูตรโครงสร้างของสารประกอบ สูตรโครงสร้างของสารให้เลขอะตอมของแต่ละองค์ประกอบที่ประกอบเป็นสารประกอบนั้น (ข้อมูลนี้มีอยู่ในหนังสืออ้างอิงทั้งหมด) ตัวอย่างเช่นสูตรทางเคมีของกรดไฮโดรคลอริกคือ HCl; ของกลูโคสคือ C6ซ12โอ6. ด้วยสูตรโครงสร้างนี้เราสามารถกำหนดจำนวนอะตอมแต่ละชนิดที่ประกอบเป็นสารประกอบที่กำลังพิจารณาได้- โดยที่ HCl มีไฮโดรเจน 1 อะตอมและคลอรีน 1 อะตอม
- น้ำตาลกลูโคสโมเลกุลค6ซ12โอ6 มีคาร์บอน 6 อะตอมไฮโดรเจน 12 อะตอมและออกซิเจน 6 อะตอม
กำหนดอะตอมมวลเฉลี่ยขององค์ประกอบแต่ละองค์ประกอบ ใช้ตารางธาตุเพื่อหาอะตอมมวลเฉลี่ยของแต่ละองค์ประกอบที่มีอยู่ในสารประกอบ โดยปกติอะตอมมวลเฉลี่ยจะเขียนไว้ใต้สัญลักษณ์ทางเคมีของธาตุบนตารางธาตุ คล้ายกับการคำนวณมวลโมลาร์ของธาตุให้คูณอะตอมมวลเฉลี่ย 1 กรัม / โมล
- อะตอมมวลเฉลี่ยของธาตุที่ประกอบเป็นกรดไฮโดรคลอริกมีดังนี้ไฮโดรเจน 1,007 ก. / โมลและคลอรีน 35,453 ก. / โมล
- อะตอมมวลเฉลี่ยของธาตุที่ประกอบกันเป็นโมเลกุลของกลูโคสคือคาร์บอน 12,017 กรัม / โมล ไฮโดรเจน 1,007 กรัม / โมล; และออกซิเจน 15.9995 กรัม / โมล
คำนวณมวลโมลาร์ของแต่ละองค์ประกอบ การคูณอะตอมมวลของธาตุด้วยจำนวนอะตอมที่ก่อให้เกิดในสารประกอบจะทำให้มวลเฉลี่ยของธาตุในสารประกอบ
- ในกรณีของกรดไฮโดรคลอริก HCl มวลโมลาร์ของธาตุไฮโดรเจนคือ 1,007 กรัม / โมลและคลอรีนคือ 35,453 กรัม / โมล
- ในกรณีของกลูโคสค6ซ12โอ6มวลโมลาร์ของแต่ละองค์ประกอบมีดังนี้: คาร์บอน 12,0107 x 6 = 72,0642 g / mol; ไฮโดรเจน 1,007 x 12 = 12,084 g / mol; ออกซิเจน 15,9995 x 6 = 95,9964 g / mol
มวลโมลาร์ทั้งหมดขององค์ประกอบที่เป็นส่วนประกอบ มวลโมลาร์ทั้งหมดขององค์ประกอบปุ๋ยหมักคือมวลโมลาร์ของสารประกอบในขั้นตอนก่อนหน้านี้เราคำนวณมวลโมลาร์ของแต่ละองค์ประกอบที่มีอยู่ในสารประกอบในขั้นตอนนี้เราต้องบวกค่าทั้งหมดเหล่านี้เข้าด้วยกัน
- มวลโมเลกุลของกรดไฮโดรคลอริกคือ 1,007 + 35,453 = 36,460 g / mol 36.46 กรัมคือมวลของกรดไฮโดรคลอริก 1 โมล
- มวลโมเลกุลของกลูโคสเท่ากับ 72,0642 + 12,084 + 95,9964 = 180,1446 g / mol ดังนั้นกลูโคสแต่ละโมลจึงมีมวล 180.14 กรัม
คำแนะนำ
- แม้ว่าในกรณีส่วนใหญ่อะตอมมวลเฉลี่ยจะถูกบันทึกไว้ใกล้ที่สุด 1 ส่วน 1,000 (ทศนิยม 4 ตำแหน่ง) ในห้องปฏิบัติการมวลโมลาร์มักจะลดลงเหลือ 2 ตำแหน่งทศนิยม บางครั้งก็น้อยกว่าสำหรับโมเลกุลขนาดใหญ่ ดังนั้นในกรณีของห้องปฏิบัติการมวลโมลาร์ของกรดไฮโดรคลอริกอาจเขียนเป็น 36.46 กรัมต่อโมลสำหรับกลูโคส 180.14 กรัมต่อโมล
สิ่งที่คุณต้องการ
- หนังสืออ้างอิงทางเคมีหรือตารางธาตุ
- คอมพิวเตอร์



