ผู้เขียน:
Helen Garcia
วันที่สร้าง:
21 เมษายน 2021
วันที่อัปเดต:
1 กรกฎาคม 2024

เนื้อหา
สมการเคมีคือการแสดงสัญลักษณ์ของปฏิกิริยาเคมี ในกรณีนี้ สารประกอบที่ทำปฏิกิริยา (รีเอเจนต์) จะถูกเขียนไว้ทางด้านซ้าย และสารที่เป็นผลลัพธ์ (ผลิตภัณฑ์จากปฏิกิริยา) จะอยู่ทางด้านขวาของสมการ ลูกศรวางระหว่างพวกเขาจากซ้ายไปขวาซึ่งระบุทิศทางของปฏิกิริยา ตามกฎการอนุรักษ์มวล ในระหว่างปฏิกิริยาเคมี อะตอมใหม่จะไม่ปรากฏขึ้นหรืออะตอมเก่าหายไป ดังนั้นจำนวนอะตอมในสารตั้งต้นจะต้องเท่ากับจำนวนอะตอมในผลิตภัณฑ์ของปฏิกิริยาเคมี . บทความนี้จะอธิบายวิธีการปรับสมดุลสมการเคมีโดยใช้วิธีการต่างๆ
ขั้นตอน
วิธีที่ 1 จาก 2: วิธีดั้งเดิม
 1 เขียนสมการเคมี. ให้พิจารณาปฏิกิริยาต่อไปนี้เป็นตัวอย่าง:
1 เขียนสมการเคมี. ให้พิจารณาปฏิกิริยาต่อไปนี้เป็นตัวอย่าง: - ค3NS8 + โอ2 -> H2O + CO2
- ปฏิกิริยานี้อธิบายการเผาไหม้ของโพรเพน (C3NS8) ในที่ที่มีออกซิเจนกลายเป็นน้ำและคาร์บอนไดออกไซด์ (คาร์บอนไดออกไซด์)
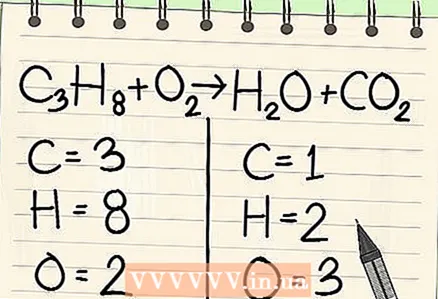 2 จดจำนวนอะตอมของแต่ละธาตุ ทำเช่นนี้กับทั้งสองข้างของสมการ สังเกตตัวห้อยที่อยู่ถัดจากแต่ละองค์ประกอบเพื่อกำหนดจำนวนอะตอมทั้งหมด จดสัญลักษณ์ของแต่ละองค์ประกอบในสมการและสังเกตจำนวนอะตอมที่เกี่ยวข้อง
2 จดจำนวนอะตอมของแต่ละธาตุ ทำเช่นนี้กับทั้งสองข้างของสมการ สังเกตตัวห้อยที่อยู่ถัดจากแต่ละองค์ประกอบเพื่อกำหนดจำนวนอะตอมทั้งหมด จดสัญลักษณ์ของแต่ละองค์ประกอบในสมการและสังเกตจำนวนอะตอมที่เกี่ยวข้อง - ตัวอย่างเช่น ทางด้านขวาของสมการที่กำลังพิจารณา จากการบวก เราจะได้ออกซิเจน 3 อะตอม
- ทางด้านซ้าย เรามีคาร์บอน 3 อะตอม (C3), 8 ไฮโดรเจนอะตอม (H8) และออกซิเจน 2 อะตอม (O2).
- ทางด้านขวา เรามีคาร์บอน 1 อะตอม (C), ไฮโดรเจน 2 อะตอม (H2) และออกซิเจน 3 อะตอม (O + O2).
 3 เก็บไฮโดรเจนและออกซิเจนไว้ใช้ในภายหลัง เนื่องจากเป็นส่วนหนึ่งของสารประกอบต่างๆ ทางด้านซ้ายและด้านขวา ไฮโดรเจนและออกซิเจนเป็นส่วนหนึ่งของโมเลกุลหลายชนิด ดังนั้นจึงควรรักษาสมดุลให้คงอยู่นานที่สุด
3 เก็บไฮโดรเจนและออกซิเจนไว้ใช้ในภายหลัง เนื่องจากเป็นส่วนหนึ่งของสารประกอบต่างๆ ทางด้านซ้ายและด้านขวา ไฮโดรเจนและออกซิเจนเป็นส่วนหนึ่งของโมเลกุลหลายชนิด ดังนั้นจึงควรรักษาสมดุลให้คงอยู่นานที่สุด - ก่อนสร้างสมดุลระหว่างไฮโดรเจนกับออกซิเจน คุณจะต้องนับอะตอมใหม่อีกครั้ง เนื่องจากอาจจำเป็นต้องมีปัจจัยเพิ่มเติมเพื่อปรับสมดุลธาตุอื่นๆ
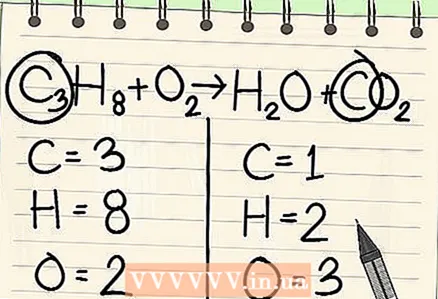 4 เริ่มต้นด้วยรายการที่มีความถี่น้อยที่สุด หากคุณต้องการสร้างสมดุลขององค์ประกอบหลายอย่าง ให้เลือกองค์ประกอบที่เป็นส่วนหนึ่งของโมเลกุลตัวทำปฏิกิริยาและหนึ่งโมเลกุลของผลิตภัณฑ์ปฏิกิริยา ดังนั้น คาร์บอนต้องสมดุลก่อน
4 เริ่มต้นด้วยรายการที่มีความถี่น้อยที่สุด หากคุณต้องการสร้างสมดุลขององค์ประกอบหลายอย่าง ให้เลือกองค์ประกอบที่เป็นส่วนหนึ่งของโมเลกุลตัวทำปฏิกิริยาและหนึ่งโมเลกุลของผลิตภัณฑ์ปฏิกิริยา ดังนั้น คาร์บอนต้องสมดุลก่อน 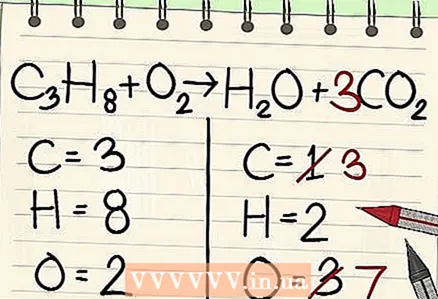 5 เพื่อความสมดุล ให้เพิ่มปัจจัยที่ด้านหน้าของอะตอมคาร์บอนเดี่ยว ใส่ปัจจัยหน้าคาร์บอนเดี่ยวทางด้านขวาของสมการเพื่อให้สมดุลกับคาร์บอน 3 ตัวทางด้านซ้าย
5 เพื่อความสมดุล ให้เพิ่มปัจจัยที่ด้านหน้าของอะตอมคาร์บอนเดี่ยว ใส่ปัจจัยหน้าคาร์บอนเดี่ยวทางด้านขวาของสมการเพื่อให้สมดุลกับคาร์บอน 3 ตัวทางด้านซ้าย - ค3NS8 + โอ2 -> H2O + 3CO2
- ตัวประกอบของ 3 ที่ด้านหน้าของคาร์บอนทางด้านขวาของสมการบ่งชี้ว่ามีอะตอมของคาร์บอนอยู่สามอะตอม ซึ่งสอดคล้องกับอะตอมของคาร์บอนสามตัวในโมเลกุลโพรเพนทางด้านซ้าย
- ในสมการทางเคมี คุณสามารถเปลี่ยนสัมประสิทธิ์ที่อยู่หน้าอะตอมและโมเลกุลได้ แต่ตัวห้อยจะต้องไม่เปลี่ยนแปลง
 6 จากนั้นให้สมดุลอะตอมไฮโดรเจน หลังจากที่คุณปรับจำนวนอะตอมของคาร์บอนทางด้านซ้ายและด้านขวาให้เท่ากันแล้ว ไฮโดรเจนและออกซิเจนก็ยังคงไม่สมดุล ด้านซ้ายของสมการมีอะตอมไฮโดรเจน 8 อะตอม เลขเดียวกันควรอยู่ทางขวา บรรลุสิ่งนี้ด้วยอัตราส่วน
6 จากนั้นให้สมดุลอะตอมไฮโดรเจน หลังจากที่คุณปรับจำนวนอะตอมของคาร์บอนทางด้านซ้ายและด้านขวาให้เท่ากันแล้ว ไฮโดรเจนและออกซิเจนก็ยังคงไม่สมดุล ด้านซ้ายของสมการมีอะตอมไฮโดรเจน 8 อะตอม เลขเดียวกันควรอยู่ทางขวา บรรลุสิ่งนี้ด้วยอัตราส่วน - ค3NS8 + โอ2 -> 4H2O + 3CO2
- เราได้เพิ่มตัวประกอบเป็น 4 ทางด้านขวา เนื่องจากตัวห้อยแสดงว่าเรามีไฮโดรเจนสองอะตอมอยู่แล้ว
- หากคุณคูณตัวประกอบ 4 ด้วยตัวห้อย 2 คุณจะได้ 8
- เป็นผลให้ได้รับออกซิเจน 10 อะตอมทางด้านขวา: 3x2 = 6 อะตอมในโมเลกุล 3CO สามตัว2 และอีกสี่อะตอมในสี่โมเลกุลของน้ำ
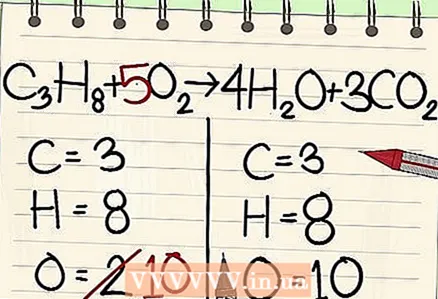 7 ปรับสมดุลอะตอมออกซิเจน อย่าลืมคำนึงถึงสัมประสิทธิ์ที่คุณใช้เพื่อทำให้อะตอมอื่นสมดุล เนื่องจากคุณเพิ่มสัมประสิทธิ์หน้าโมเลกุลทางด้านขวาของสมการ จำนวนอะตอมออกซิเจนจึงเปลี่ยนไป ตอนนี้คุณมีออกซิเจน 4 อะตอมในโมเลกุลของน้ำ และ 6 อะตอมออกซิเจนในโมเลกุลคาร์บอนไดออกไซด์ ดังนั้นจึงมีออกซิเจน 10 อะตอมทางด้านขวา
7 ปรับสมดุลอะตอมออกซิเจน อย่าลืมคำนึงถึงสัมประสิทธิ์ที่คุณใช้เพื่อทำให้อะตอมอื่นสมดุล เนื่องจากคุณเพิ่มสัมประสิทธิ์หน้าโมเลกุลทางด้านขวาของสมการ จำนวนอะตอมออกซิเจนจึงเปลี่ยนไป ตอนนี้คุณมีออกซิเจน 4 อะตอมในโมเลกุลของน้ำ และ 6 อะตอมออกซิเจนในโมเลกุลคาร์บอนไดออกไซด์ ดังนั้นจึงมีออกซิเจน 10 อะตอมทางด้านขวา - บวกตัวประกอบของ 5 ให้กับโมเลกุลออกซิเจนทางด้านซ้ายของสมการ แต่ละชิ้นมีอะตอมออกซิเจน 10 อะตอม
- ค3NS8 + 5O2 -> 4H2O + 3CO2.

- ดังนั้น สมการทั้งสองข้างจึงมีจำนวนอะตอมของคาร์บอน ไฮโดรเจน และออกซิเจนเท่ากัน สมการมีความสมดุล
วิธีที่ 2 จาก 2: วิธีพีชคณิต
- 1 เขียนสมการปฏิกิริยา ตัวอย่างเช่น ให้พิจารณาปฏิกิริยาเคมีต่อไปนี้:
- บมจ5 + โฮ2O -> H3ป4 + HCl
- 2 ใส่จดหมายไว้ข้างหน้าของการเชื่อมต่อแต่ละครั้ง:
- NSบมจ5 + NSNS2โอ -> คNS3ป4 + NSHCl
- 3 ทำให้จำนวนอะตอมเท่ากันสำหรับแต่ละองค์ประกอบทางด้านซ้ายและด้านขวาของสมการ
- NSบมจ5 + NSNS2โอ -> คNS3ป4 + NSHCl
- ทางด้านซ้ายเรามี2NS อะตอมไฮโดรเจน (2 ในแต่ละH2O) ในขณะที่ด้านขวาคือ3ค+NS อะตอมไฮโดรเจน (3 ในแต่ละH3ป4 และ 1 ในแต่ละโมเลกุล HCl) เนื่องจากด้านซ้ายและด้านขวาต้องมีไฮโดรเจนอะตอมเท่ากัน 2NS ควรเท่ากับ3ค+NS.
- ทำสิ่งนี้กับองค์ประกอบทั้งหมด:
- NS: NS=ค
- Cl: 5NS=NS
- H: 2NS=3ค+NS
- 4 แก้ระบบสมการเพื่อหาค่าตัวเลขของสัมประสิทธิ์ ระบบมีคำตอบหลายคำตอบ เนื่องจากมีตัวแปรมากกว่าสมการ จำเป็นต้องหาวิธีแก้ปัญหาดังกล่าวเพื่อให้สัมประสิทธิ์ทั้งหมดอยู่ในรูปของจำนวนเต็มที่น้อยที่สุดที่เป็นไปได้
- ในการแก้ระบบสมการอย่างรวดเร็ว ให้กำหนดค่าตัวเลขให้กับตัวแปรตัวใดตัวหนึ่ง สมมติว่า a = 1 มาแก้ระบบและหาค่าของตัวแปรที่เหลือ:
- สำหรับ P a = c ดังนั้น c = 1
- สำหรับ Cl 5a = d ดังนั้น d = 5
- เนื่องจากสำหรับ H 2b = 3c + d เราพบค่า b:
- 2b = 3 (1) + 5
- 2b = 3 + 5
- 2b = 8
- ข = 4
- ดังนั้นเราจึงมีค่าสัมประสิทธิ์ดังต่อไปนี้:
- a = 1
- ข = 4
- ค = 1
- d = 5
เคล็ดลับ
- หากคุณประสบปัญหา คุณสามารถใช้เครื่องคำนวณออนไลน์เพื่อปรับสมดุลสมการเคมีได้ อย่างไรก็ตาม โปรดทราบว่าไม่อนุญาตให้ใช้เครื่องคิดเลขดังกล่าวระหว่างการสอบ ดังนั้นอย่าพึ่งพาเครื่องคิดเลขเพียงอย่างเดียว
- จำไว้ว่าบางครั้งสมการก็ทำให้ง่ายขึ้นได้! หากสัมประสิทธิ์ทั้งหมดหารด้วยจำนวนเต็มลงตัว ให้ลดสมการลง
คำเตือน
- ในการกำจัดสัมประสิทธิ์เศษส่วน ให้คูณสมการทั้งหมด (ด้านซ้ายและขวา) ด้วยตัวส่วนของเศษส่วน
- ห้ามใช้เศษส่วนเป็นค่าสัมประสิทธิ์ของสมการเคมี เนื่องจากปฏิกิริยาเคมีไม่มีโมเลกุลหรืออะตอมครึ่งหนึ่ง
- ในกระบวนการดุลยภาพ คุณสามารถใช้เศษส่วนเพื่อความสะดวก แต่สมการจะไม่สมดุลตราบเท่าที่มีค่าสัมประสิทธิ์เศษส่วนอยู่ในนั้น



