ผู้เขียน:
Christy White
วันที่สร้าง:
8 พฤษภาคม 2021
วันที่อัปเดต:
1 กรกฎาคม 2024

เนื้อหา
- ที่จะก้าว
- วิธีที่ 1 จาก 3: ส่วนที่หนึ่ง: การทำความเข้าใจเกี่ยวกับเปลือกอิเล็กตรอน
- วิธีที่ 2 จาก 3: ส่วนที่สอง: การค้นหาวาเลนซ์อิเล็กตรอนในโลหะยกเว้นโลหะที่เปลี่ยนผ่าน
- วิธีที่ 3 จาก 3: ส่วนที่สาม: การค้นหาวาเลนซ์อิเล็กตรอนในโลหะการเปลี่ยนผ่าน
- เคล็ดลับ
- ความจำเป็น
วาเลนซ์อิเล็กตรอนอยู่ในเปลือกนอกขององค์ประกอบ จำนวนเวเลนซ์อิเล็กตรอนในอะตอมเป็นตัวกำหนดชนิดของพันธะเคมีที่องค์ประกอบนี้สามารถก่อตัวได้ วิธีที่ดีที่สุดในการหาจำนวนเวเลนซ์อิเล็กตรอนคือการใช้ตารางธาตุของธาตุ
ที่จะก้าว
วิธีที่ 1 จาก 3: ส่วนที่หนึ่ง: การทำความเข้าใจเกี่ยวกับเปลือกอิเล็กตรอน
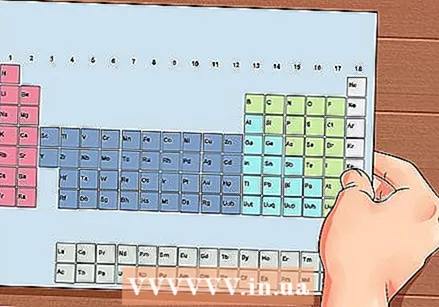 ตารางธาตุ นี่คือตารางที่มีรหัสสีซึ่งในแต่ละเซลล์องค์ประกอบจะแสดงด้วยเลขอะตอมและตัวอักษร 1 ถึง 3 ตัวเป็นสัญลักษณ์
ตารางธาตุ นี่คือตารางที่มีรหัสสีซึ่งในแต่ละเซลล์องค์ประกอบจะแสดงด้วยเลขอะตอมและตัวอักษร 1 ถึง 3 ตัวเป็นสัญลักษณ์ 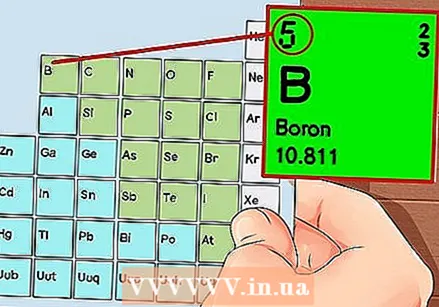 ค้นหาเลขอะตอมของธาตุ เลขอะตอมอยู่ด้านบนหรือถัดจากสัญลักษณ์ขององค์ประกอบ ตัวอย่างเช่นโบรอน (B) มีเลขอะตอม 5 ซึ่งหมายความว่ามีโปรตอน 5 ตัวและอิเล็กตรอน 5 ตัว
ค้นหาเลขอะตอมของธาตุ เลขอะตอมอยู่ด้านบนหรือถัดจากสัญลักษณ์ขององค์ประกอบ ตัวอย่างเช่นโบรอน (B) มีเลขอะตอม 5 ซึ่งหมายความว่ามีโปรตอน 5 ตัวและอิเล็กตรอน 5 ตัว 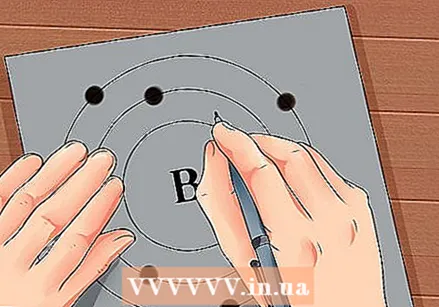 วาดภาพแทนอะตอมอย่างง่าย ๆ และวางอิเล็กตรอนในวงโคจรรอบนิวเคลียส งานเหล่านี้เรียกอีกอย่างว่าระดับเปลือกหอยหรือระดับพลังงาน จำนวนอิเล็กตรอนสูงสุดที่สามารถอยู่ในเปลือกเดียวกันได้รับการแก้ไขและเปลือกจะเต็มจากวงโคจรด้านในไปยังวงโคจรด้านนอก
วาดภาพแทนอะตอมอย่างง่าย ๆ และวางอิเล็กตรอนในวงโคจรรอบนิวเคลียส งานเหล่านี้เรียกอีกอย่างว่าระดับเปลือกหอยหรือระดับพลังงาน จำนวนอิเล็กตรอนสูงสุดที่สามารถอยู่ในเปลือกเดียวกันได้รับการแก้ไขและเปลือกจะเต็มจากวงโคจรด้านในไปยังวงโคจรด้านนอก - K Shell (ด้านใน): สูงสุด 2 อิเล็กตรอน
- L Shell: สูงสุด 8 อิเล็กตรอน
- M Shell: สูงสุด 18 อิเล็กตรอน
- N Shell: สูงสุด 32 อิเล็กตรอน
- O Shell: สูงสุด 50 อิเล็กตรอน
- P Shell (ด้านนอก): สูงสุด 72 อิเล็กตรอน
 ค้นหาจำนวนอิเล็กตรอนในเปลือกนอก เหล่านี้คือเวเลนซ์อิเล็กตรอน
ค้นหาจำนวนอิเล็กตรอนในเปลือกนอก เหล่านี้คือเวเลนซ์อิเล็กตรอน - เมื่อวาเลนซ์เชลล์เต็มองค์ประกอบจะคงที่
- ถ้าเปลือกวาเลนซ์ไม่เต็มองค์ประกอบนั้นจะมีปฏิกิริยาซึ่งหมายความว่ามันสามารถเชื่อมโยงทางเคมีกับอะตอมของธาตุอื่นได้ แต่ละอะตอมแบ่งปันเวเลนซ์อิเล็กตรอนเพื่อพยายามทำให้เวเลนซ์เชลล์เต็ม
วิธีที่ 2 จาก 3: ส่วนที่สอง: การค้นหาวาเลนซ์อิเล็กตรอนในโลหะยกเว้นโลหะที่เปลี่ยนผ่าน
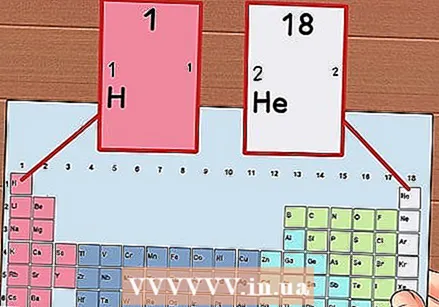 หมายเลขแต่ละคอลัมน์ของตารางธาตุตั้งแต่ 1 ถึง 18 ไฮโดรเจน (H) อยู่ที่ด้านบนสุดของคอลัมน์ 1 และฮีเลียม (He) ที่ด้านบนสุดของคอลัมน์ 18 ซึ่งเป็นกลุ่มธาตุต่างๆ
หมายเลขแต่ละคอลัมน์ของตารางธาตุตั้งแต่ 1 ถึง 18 ไฮโดรเจน (H) อยู่ที่ด้านบนสุดของคอลัมน์ 1 และฮีเลียม (He) ที่ด้านบนสุดของคอลัมน์ 18 ซึ่งเป็นกลุ่มธาตุต่างๆ 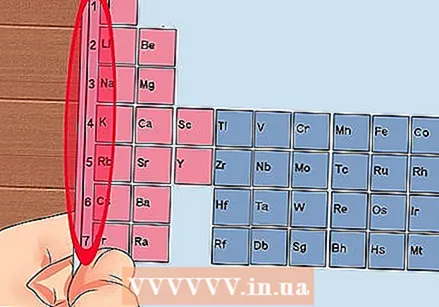 ให้ตัวเลขแต่ละแถวตั้งแต่ 1 ถึง 7 นี่คือช่วงเวลาขององค์ประกอบและสอดคล้องกับจำนวนของเปลือกหอยหรือระดับพลังงานของอะตอม
ให้ตัวเลขแต่ละแถวตั้งแต่ 1 ถึง 7 นี่คือช่วงเวลาขององค์ประกอบและสอดคล้องกับจำนวนของเปลือกหอยหรือระดับพลังงานของอะตอม - ไฮโดรเจน (H) และฮีเลียม (He) มี 1 เชลล์ในขณะที่ฟรังเซียม (Fr) มี 7
- แลนทาไนด์และแอกติไนด์ถูกจัดกลุ่มและแสดงอยู่ด้านล่างตารางหลัก แลนทาไนด์ทั้งหมดอยู่ในคาบที่ 6 กลุ่มที่ 3 และแอคติไนด์ทั้งหมดอยู่ในคาบที่ 7 กลุ่มที่ 3
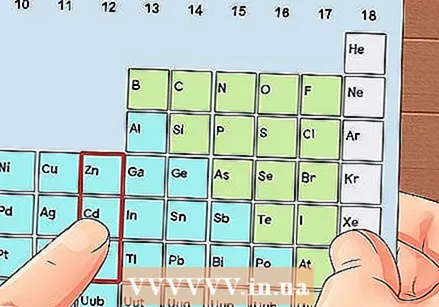 ค้นหาองค์ประกอบที่ไม่ใช่โลหะทรานซิชัน โลหะทรานซิชั่นอยู่ในกลุ่ม 3 ถึง 12 หมายเลขกลุ่มของโลหะอื่นระบุจำนวนเวเลนซ์อิเล็กตรอน
ค้นหาองค์ประกอบที่ไม่ใช่โลหะทรานซิชัน โลหะทรานซิชั่นอยู่ในกลุ่ม 3 ถึง 12 หมายเลขกลุ่มของโลหะอื่นระบุจำนวนเวเลนซ์อิเล็กตรอน - กลุ่มที่ 1: 1 เวเลนซ์อิเล็กตรอน
- กลุ่มที่ 2: เวเลนซ์อิเล็กตรอน 2 ตัว
- กลุ่มที่ 13: วาเลนซ์อิเล็กตรอน 3 ตัว
- กลุ่มที่ 14: เวเลนซ์อิเล็กตรอน 4 ตัว
- กลุ่มที่ 15: เวเลนซ์อิเล็กตรอน 5 ตัว
- กลุ่ม 16: 6 เวเลนซ์อิเล็กตรอน
- กลุ่มที่ 17: เวเลนซ์อิเล็กตรอน 7 ตัว
- กลุ่มที่ 18: 8 เวเลนซ์อิเล็กตรอน - ยกเว้นฮีเลียมซึ่งมี 2
วิธีที่ 3 จาก 3: ส่วนที่สาม: การค้นหาวาเลนซ์อิเล็กตรอนในโลหะการเปลี่ยนผ่าน
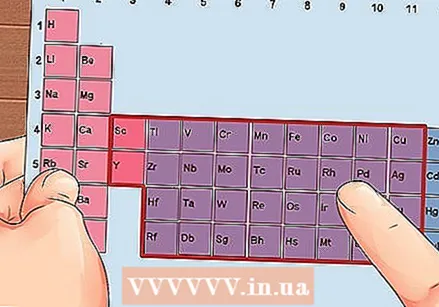 ค้นหาองค์ประกอบจากกลุ่ม 3 ถึง 12 โลหะทรานซิชัน
ค้นหาองค์ประกอบจากกลุ่ม 3 ถึง 12 โลหะทรานซิชัน กำหนดจำนวนเวเลนซ์อิเล็กตรอนตามหมายเลขกลุ่ม หมายเลขกลุ่มเหล่านี้สอดคล้องกับจำนวนเวเลนซ์อิเล็กตรอนที่เป็นไปได้
กำหนดจำนวนเวเลนซ์อิเล็กตรอนตามหมายเลขกลุ่ม หมายเลขกลุ่มเหล่านี้สอดคล้องกับจำนวนเวเลนซ์อิเล็กตรอนที่เป็นไปได้ - กลุ่มที่ 3: เวเลนซ์อิเล็กตรอน 3 ตัว
- กลุ่มที่ 4: 2 ถึง 4 เวเลนซ์อิเล็กตรอน
- กลุ่มที่ 5: 2 ถึง 5 เวเลนซ์อิเล็กตรอน
- กลุ่มที่ 6: 2 ถึง 6 เวเลนซ์อิเล็กตรอน
- กลุ่มที่ 7: 2 ถึง 7 เวเลนซ์อิเล็กตรอน
- กลุ่มที่ 8: 2 หรือ 3 เวเลนซ์อิเล็กตรอน
- กลุ่มที่ 9: 2 หรือ 3 เวเลนซ์อิเล็กตรอน
- กลุ่ม 10: 2 หรือ 3 เวเลนซ์อิเล็กตรอน
- กลุ่มที่ 11: 1 หรือ 2 เวเลนซ์อิเล็กตรอน
- กลุ่ม 12: 2 เวเลนซ์อิเล็กตรอน
เคล็ดลับ
- โลหะทรานซิชั่นอาจมีเปลือกวาเลนซ์ที่ไม่เต็มสมบูรณ์ การกำหนดจำนวนเวเลนซ์อิเล็กตรอนที่แน่นอนในโลหะทรานซิชันจำเป็นต้องใช้หลักการบางประการของทฤษฎีควอนตัมที่อยู่นอกเหนือขอบเขตของบทความนี้
ความจำเป็น
- ตารางธาตุ
- ดินสอ
- กระดาษ