ผู้เขียน:
Lewis Jackson
วันที่สร้าง:
12 พฤษภาคม 2021
วันที่อัปเดต:
1 กรกฎาคม 2024

เนื้อหา
การกำหนดจำนวนนิวตรอนในอะตอมนั้นค่อนข้างง่ายคุณไม่จำเป็นต้องทำการทดลองใด ๆ ในการคำนวณจำนวนนิวตรอนในอะตอมหรือไอโซโทปธรรมดาคุณต้องมีตารางธาตุให้พร้อมและทำตามคำแนะนำ
ขั้นตอน
วิธีที่ 1 จาก 2: ค้นหาจำนวนนิวตรอนในอะตอมปกติ
กำหนดตำแหน่งขององค์ประกอบบนตารางธาตุ ตัวอย่างเช่นเราจะพบธาตุออสเมียม (Os) ในแถวที่หกจากด้านบน
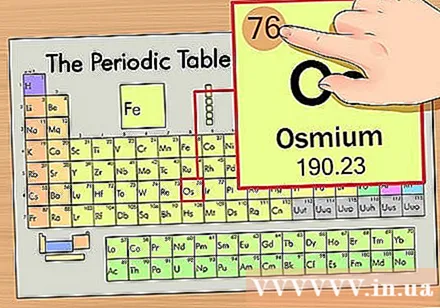
ค้นหาเลขอะตอมของธาตุ นี่คือตัวเลขที่เด่นชัดที่สุดที่อยู่ในแต่ละองค์ประกอบและอยู่เหนือสัญลักษณ์เฉพาะ (บนกระดานที่เราใช้ไม่มีตัวเลขอื่น) เลขอะตอมคือจำนวนโปรตอนในอะตอมเดียวของธาตุนั้น. Os คือเลข 76 ซึ่งหมายความว่ามีโปรตอน 76 ตัวในอะตอมของออสเมียม- จำนวนโปรตอนไม่เคยเปลี่ยนแปลงในองค์ประกอบ โดยพื้นฐานแล้วเป็นลักษณะการกำหนดขององค์ประกอบ
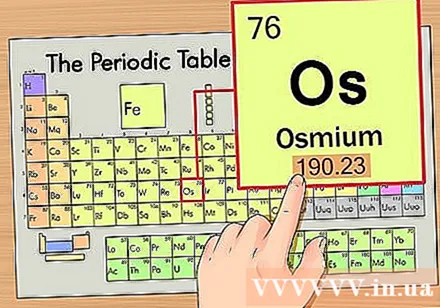
หาน้ำหนักอะตอมของธาตุ โดยปกติตัวเลขนี้จะอยู่ด้านล่างสัญลักษณ์เฉพาะ โปรดทราบว่าตารางธาตุในตัวอย่างนี้มีเพียงเลขอะตอมและไม่มีน้ำหนักอะตอม ไม่ใช่ตารางธาตุทั้งหมด ออสเมียมมีน้ำหนักอะตอม 190.23
ปัดน้ำหนักอะตอมให้เป็นจำนวนเต็มที่ใกล้ที่สุดเพื่อให้ได้มวลอะตอม ตัวอย่างเช่น 190.23 จะปัดเศษเป็น 190 ดังนั้นมวลอะตอมของออสเมียมจึงเท่ากับ 190- น้ำหนักอะตอมเป็นค่าเฉลี่ยของไอโซโทปขององค์ประกอบทางเคมีเดียวกันซึ่งโดยปกติแล้วจึงไม่เป็นจำนวนเต็ม
ลบเลขอะตอมออกจากมวลอะตอม เนื่องจากมวลอะตอมส่วนใหญ่เป็นมวลของโปรตอนและนิวตรอนการลบจำนวนโปรตอนออกจากมวลอะตอม (เช่นเลขอะตอม) คุณจะ นับ รับจำนวนนิวตรอนในอะตอม จำนวนหลังจุดทศนิยมแสดงถึงมวลที่เล็กมากของอิเล็กตรอนในอะตอม ในตัวอย่างนี้เรามี 190 (อะตอมมวล) - 76 (จำนวนโปรตอน) = 114 (จำนวนนิวตรอน)
จดจำสูตรอาหาร ในการหาจำนวนนิวตรอนเราเพียงแค่ใช้สูตรต่อไปนี้: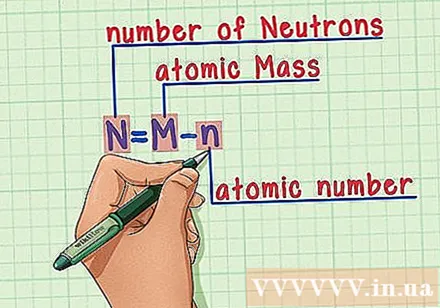
- N = M - น
- N = จำนวนนิวตรอน
- M = มวลอะตอม
- n = เลขอะตอม
- N = M - น
วิธีที่ 2 จาก 2: ค้นหาจำนวนนิวตรอนในไอโซโทป
กำหนดตำแหน่งขององค์ประกอบบนตารางธาตุ ให้เรานำไอโซโทปของธาตุคาร์บอน -14 มาเป็นตัวอย่าง เนื่องจากรูปแบบไอโซโทปของคาร์บอน -14 เป็นเพียงคาร์บอน (C) ให้มองหาคาร์บอนในตารางธาตุ (แถวที่สองจากด้านบน)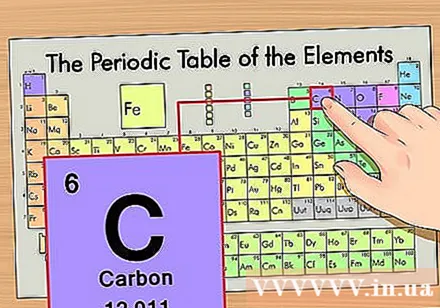
ค้นหาเลขอะตอมของธาตุ นี่คือตัวเลขที่เด่นชัดที่สุดที่อยู่ในแต่ละองค์ประกอบและอยู่เหนือสัญลักษณ์เฉพาะ (บนกระดานที่เราใช้ไม่มีตัวเลขอื่น) เลขอะตอมคือจำนวนโปรตอนในอะตอมเดียวของธาตุนั้น. C คือเลข 6 ซึ่งหมายความว่ามีโปรตอน 6 ตัวในอะตอมของคาร์บอน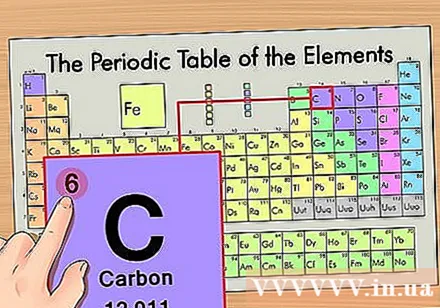
หามวลอะตอม. ไอโซโทปนี้ง่ายมากเพราะตั้งชื่อตามมวลอะตอม ตัวอย่างเช่นคาร์บอน -14 จะมีมวลอะตอมเท่ากับ 14 เมื่อคุณพบมวลอะตอมของไอโซโทปแล้วขั้นตอนที่เหลือในการค้นหาจำนวนนิวตรอนจะเหมือนกับอะตอมปกติ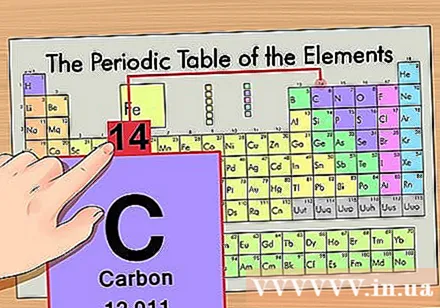
ลบเลขอะตอมออกจากมวลอะตอม เนื่องจากมวลอะตอมส่วนใหญ่เป็นมวลของโปรตอนและนิวตรอนการลบจำนวนโปรตอนออกจากมวลอะตอม (เช่นเลขอะตอม) คุณจะ นับ รับจำนวนนิวตรอนในอะตอม จำนวนหลังจุดทศนิยมแสดงถึงมวลที่เล็กมากของอิเล็กตรอนในอะตอม ในตัวอย่างนี้เรามี: 14 (อะตอมมวล) - 6 (จำนวนโปรตอน) = 8 (จำนวนนิวตรอน)
จดจำสูตรอาหาร ในการหาจำนวนนิวตรอนเราใช้สูตรต่อไปนี้: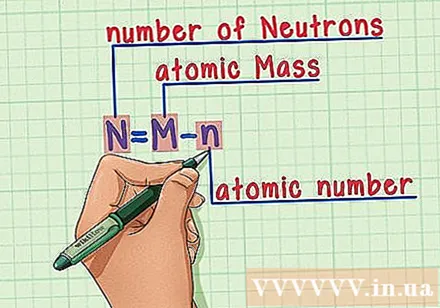
- N = M - น
- N = จำนวนนิวตรอน
- M = มวลอะตอม
- n = เลขอะตอม
- N = M - น
คำแนะนำ
- มวลขององค์ประกอบส่วนใหญ่เป็นมวลของโปรตอนและนิวตรอนในขณะที่มวลของอิเล็กตรอนและองค์ประกอบอื่น ๆ มีค่าเล็กน้อย (ใกล้เคียงกับศูนย์) เนื่องจากมวลของโปรตอนมีค่าเท่ากับมวลของนิวตรอนโดยประมาณและเลขอะตอมแทนจำนวนโปรตอนเราจึงเพียงแค่ลบจำนวนโปรตอนออกจากมวลทั้งหมด
- หากคุณจำความหมายของตัวเลขบนตารางธาตุไม่ได้โปรดจำไว้ว่าตารางธาตุมักสร้างจากเลขอะตอม (เช่นจำนวนโปรตอน) โดยเริ่มต้นที่ 1 (ไฮโดรเจน) และเพิ่มขึ้นทีละคำ จากซ้ายไปขวาลงท้ายด้วย 118 (ununoctium) เนื่องจากจำนวนโปรตอนเป็นคุณสมบัติในการระบุของแต่ละอะตอมจึงเป็นคุณสมบัติที่ง่ายที่สุดในการจัดเรียงองค์ประกอบ (ตัวอย่างเช่นอะตอมที่มีโปรตอน 2 ตัวจะเป็นฮีเลียมเสมอเช่นเดียวกับอะตอมที่มีโปรตอน 79 ตัวจะเป็นทองคำเสมอ)
แหล่งที่มาและการอ้างอิง
- ตารางธาตุแบบโต้ตอบ