ผู้เขียน:
Monica Porter
วันที่สร้าง:
17 มีนาคม 2021
วันที่อัปเดต:
1 กรกฎาคม 2024
![🧪สารละลาย 3 : โมลาร์ | โมลต่อลิตร [Chemistry#15]](https://i.ytimg.com/vi/1_O7--9W08I/hqdefault.jpg)
เนื้อหา
ความเข้มข้นของโมลาร์แสดงถึงความสัมพันธ์ระหว่างจำนวนโมลของตัวถูกละลายและปริมาตรของสารละลาย ในการคำนวณโมลาริตีคุณสามารถเริ่มต้นด้วยโมลและปริมาตรมวลและปริมาตรหรือโมลและมิลลิลิตร (มล.) จากนั้นด้วยตัวแปรข้างต้นให้ใช้สูตรความเข้มข้นของโมลาร์พื้นฐานเพื่อให้ได้ผลลัพธ์ที่ถูกต้อง
ขั้นตอน
วิธีที่ 1 จาก 4: คำนวณความเข้มข้นของโมลจากจำนวนโมลาร์และปริมาตร
สิ่งสำคัญคือต้องรู้สูตรพื้นฐานสำหรับการคำนวณความเข้มข้นของฟันกราม ความเข้มข้นของโมลเท่ากับจำนวนโมลของตัวถูกละลายหารด้วยปริมาตรของสารละลายเป็นลิตร จากนั้นเรามีสูตรต่อไปนี้: ความเข้มข้นของโมลาร์ = จำนวนโมลของตัวถูกละลาย / จำนวนลิตรของสารละลาย
- ตัวอย่าง: ความเข้มข้นของโมลาร์ของสารละลายที่มี NaCl 0.75 โมลในสารละลาย 4.2 ลิตรเป็นเท่าใด

วิเคราะห์หัวข้อ ในการคำนวณความเข้มข้นของโมลาร์คุณต้องมีจำนวนโมลและปริมาตรของสารละลายเป็นลิตร คุณไม่จำเป็นต้องคำนวณสองค่านี้เนื่องจากหัวข้อที่กำหนด- ตัวอย่างเช่น:
- จำนวนโมล = 0.75 โมลของ NaCl
- ปริมาตร = 4.2 ล
- ตัวอย่างเช่น:
หารจำนวนโมลด้วยปริมาตร ผลลัพธ์ของการแบ่งโมลตามปริมาตรคือจำนวนโมลต่อลิตรของสารละลายหรือความเข้มข้นของโมลของสารละลายนั้น
- ตัวอย่าง: ความเข้มข้นของโมลาร์ = จำนวนโมลของตัวถูกละลาย / จำนวนลิตรของสารละลาย = 0.75 โมล / 4.2 L = 0.17857142

บันทึกผลลัพธ์ของคุณ ปัดเศษเป็นสองหรือสามตัวเลขหลังเครื่องหมายจุลภาคขึ้นอยู่กับคำขอของครูหรืองานที่มอบหมาย เมื่อบันทึกผลลัพธ์ของคุณให้ย่อ "ความเข้มข้นของโมลาร์" ด้วย "M" และใส่สัญลักษณ์ทางเคมีของตัวถูกละลาย- ตัวอย่างเช่น: 0.179 M NaCl
วิธีที่ 2 จาก 4: คำนวณความเข้มข้นของโมลจากมวลและปริมาตร
จำเป็นต้องรู้สูตรพื้นฐานในการคำนวณความเข้มข้นของฟันกราม ความเข้มข้นของโมลาร์แสดงความสัมพันธ์ระหว่างจำนวนโมลของตัวถูกละลายและปริมาตรของสารละลาย สูตรสำหรับความเข้มข้นของโมลาร์มีดังนี้: ความเข้มข้นของโมลาร์ = ความเข้มข้นของตัวถูกละลาย / จำนวนลิตรของสารละลาย
- ตัวอย่างปัญหา: คำนวณจำนวนโมลของสารละลายเมื่อละลาย KMnO 3.4 กรัม4 ในน้ำ 5.2 ลิตร

วิเคราะห์หัวข้อ: ในการหาความเข้มข้นของฟันกรามคุณต้องมีจำนวนโมลและปริมาตรของสารละลายเป็นลิตร หากไม่ได้กำหนดค่าเหล่านี้ แต่คุณทราบปริมาตรและมวลของสารละลายคุณสามารถกำหนดจำนวนโมลของตัวถูกละลายก่อนที่จะคำนวณความเข้มข้นของโมลาร์- ตัวอย่างเช่น:
- น้ำหนัก = 3.4 กรัม KMnO4
- ปริมาตร = 5.2 ล
- ตัวอย่างเช่น:
คำนวณโมเลกุลมวลของตัวถูกละลาย ในการคำนวณจำนวนโมลของตัวถูกละลายจากมวลหรือกรัมของตัวถูกละลายก่อนอื่นคุณต้องกำหนดโมเลกุลมวลของตัวถูกละลาย โมเลกุลมวลของตัวถูกละลายสามารถกำหนดได้โดยการเพิ่มอะตอมมวลของแต่ละองค์ประกอบในสารละลาย ในการหาลูกบาศก์อะตอมของแต่ละองค์ประกอบให้ใช้ตารางธาตุ
- ตัวอย่างเช่น:
- อะตอมมวลของ K = 39.1 ก
- มวลอะตอมของ Mn = 54,9 g
- มวลอะตอมของ O = 16,0 ก
- รวมอะตอมของมวล = K + Mn + O + O + O + O = 39.1 + 54.9 + 16 + 16 + 16 + 16 = 158.0 ก
- ตัวอย่างเช่น:
แปลงกรัมเป็นโมล เมื่อคุณมีมวลโมลาร์แล้วคุณต้องคูณจำนวนกรัมของตัวถูกละลายในสารละลายด้วยปัจจัยการแปลงเทียบเท่า 1 โมลต่อมวลโมลาร์ของตัวถูกละลาย ผลลัพธ์ของการคูณนี้คือจำนวนโมลของตัวถูกละลาย
- ตัวอย่าง: กรัมของตัวถูกละลาย * (1 / มวลโมลาร์ของตัวถูกละลาย) = 3.4 g * (1 mol / 158 g) = 0.0215 mol
หารจำนวนโมลด้วยจำนวนลิตร ตอนนี้คุณได้คำนวณจำนวนโมลแล้วตอนนี้หารจำนวนนั้นด้วยปริมาตรของสารละลายเป็นลิตรคุณจะมีความเข้มข้นของโมลของสารละลายนั้น
- ตัวอย่าง: ความเข้มข้นของโมลาร์ = จำนวนโมลของตัวถูกละลาย / จำนวนลิตรของสารละลาย = 0.0215 mol / 5.2 L = 0.004134615
บันทึกผลลัพธ์ของคุณ คุณต้องปัดเศษผลลัพธ์ตามที่ครูกำหนดโดยปกติจะเป็นตัวเลข 2-3 ตัวหลังเครื่องหมายจุลภาค นอกจากนี้เมื่อเขียนผลลัพธ์ให้ย่อ "ความเข้มข้นของโมลาร์" เป็น "M" พร้อมกับสัญลักษณ์ทางเคมีของตัวถูกละลาย
- ตัวอย่างเช่น: 0.004 ล้านกม4
วิธีที่ 3 จาก 4: คำนวณความเข้มข้นของโมลจากจำนวนโมลและมิลลิลิตรของสารละลาย
จำเป็นต้องรู้สูตรสำหรับความเข้มข้นของฟันกราม เพื่อคำนวณความเข้มข้นของฟันกราม คุณต้องคำนวณจำนวนโมลของตัวถูกละลายต่อลิตรของสารละลายไม่ใช่มิลลิลิตรของสารละลาย สูตรทั่วไปสำหรับการคำนวณความเข้มข้นของโมลาร์คือ: ความเข้มข้นของโมลาร์ = จำนวนโมลของตัวถูกละลาย / จำนวนลิตรของสารละลาย
- ตัวอย่าง: คำนวณความเข้มข้นของโมลาร์ของสารละลายที่มี CaCl 1.2 โมล2 ในน้ำ 2905 มิลลิลิตร
วิเคราะห์หัวข้อ ในการคำนวณความเข้มข้นของโมลาร์คุณต้องมีจำนวนโมลของตัวถูกละลายและปริมาตรของสารละลายเป็นลิตร หากกำหนดปริมาตรของสารละลายในโจทย์เป็นมิลลิลิตรให้แปลงปริมาตรที่เท่ากันเป็นลิตรก่อนทำการคำนวณ
- ตัวอย่างเช่น:
- จำนวนโมล = 1.2 โมลของ CaCl2
- ปริมาตร = 2905 มล
- ตัวอย่างเช่น:
แปลงมิลลิลิตรเป็นลิตร ในการแปลงสารละลายจากมิลลิลิตรเป็นลิตรให้หารจำนวนมิลลิลิตรด้วย 1,000 เนื่องจากแต่ละลิตรมีค่าเท่ากับ 1,000 มิลลิลิตร คุณยังสามารถแปลงมิลลิลิตรเป็นลิตรได้โดยเลื่อนจุดทศนิยมไปทางซ้าย 3 หลัก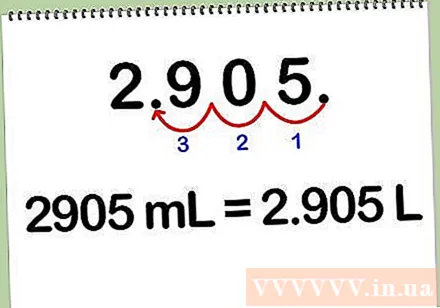
- ตัวอย่างเช่น 2905 ml * (1 L / 1000 ml) = 2,905 L
หารจำนวนโมลด้วยจำนวนลิตร หลังจากที่คุณมีจำนวนลิตรแล้วคุณสามารถคำนวณความเข้มข้นของโมลได้โดยหารจำนวนโมลด้วยจำนวนลิตรของสารละลาย
- ตัวอย่าง: ความเข้มข้นของโมลาร์ = จำนวนโมลของตัวถูกละลาย / จำนวนลิตรของสารละลาย = 1.2 โมลของ CaCl2 / 2,905 L = 0.413080895
บันทึกผลลัพธ์ของคุณ อย่าลืมปัดเศษผลลัพธ์เป็นสองหรือสามลูกน้ำหรือตามที่ครูร้องขอ เมื่อบันทึกผลลัพธ์ให้ย่อ "ความเข้มข้นของโมลาร์" เป็น "M" แล้วตามด้วยสัญลักษณ์ทางเคมีสำหรับตัวถูกละลาย
- ตัวอย่างเช่น: 0.413 M CaCl2
วิธีที่ 4 จาก 4: การฝึกฝนเพิ่มเติม
คำนวณความเข้มข้นของสารละลายเมื่อ NaCl 5.2 กรัมละลายในน้ำ 800 มล. กำหนดค่าที่โจทย์ให้มา: มวลเป็นกรัมและปริมาตรเป็นมิลลิลิตร
- มวล = 5.2 กรัม NaCl
- ปริมาตร = น้ำ 800 มล
ค้นหาโมเลกุลมวลของ NaCl โดยการเพิ่มลูกบาศก์อะตอมของธาตุ Na และลูกบาศก์อะตอมของ Cl
- อะตอมมวลของ Na = 22.99 g
- มวลอะตอมของ Cl = 35.45 g
- มวลโมเลกุลของ NaCl = 22.99 + 35.45 = 58.44 g
คูณมวลของตัวถูกละลายด้วยปัจจัยการแปลงโมลาร์ ในตัวอย่างนี้มวลโมเลกุลของ NaCl คือ 58.44 กรัมดังนั้นปัจจัยการแปลงคือ "1 mol / 58.44 g"
- จำนวน NaCl โมล = 5.2 g NaCl * (1 mol / 58.44 g) = 0.8898 mol = 0.09 mol
แบ่งน้ำ 800 มล. คูณ 1,000 คุณจะได้ปริมาตรน้ำเป็นลิตร
- คุณยังสามารถคูณ 800 มล. ด้วยตัวประกอบการแปลง 1 ลิตร / 1,000 มล. จากมิลลิลิตรเป็นลิตร
- หากต้องการลดขั้นตอนการคูณให้สั้นลงคุณสามารถกลับจุดทศนิยม 3 หลักไปทางซ้าย
- ปริมาตร = 800 ml * (1 L / 1,000 ml) = 800 ml / 1000 ml = 0.8 L
หารจำนวนโมลของตัวถูกละลายด้วยปริมาตรของสารละลายเป็นลิตร ในการคำนวณความเข้มข้นของโมลาร์คุณต้องหาร 0.09 โมลของตัวถูกละลาย (ในกรณีนี้คือ NaCl) ด้วยปริมาตรของสารละลายเป็นลิตร
- ความเข้มข้นของโมลาร์ = จำนวนโมลของตัวถูกละลาย / จำนวนลิตรของสารละลาย = 0.09 mol / 0.8 L = 0.1125 mol / L
บันทึกผลลัพธ์สุดท้าย ปัดผลลัพธ์เป็นตัวเลขสองหรือสามตัวหลังเครื่องหมายจุลภาคและย่อ "ความเข้มข้นของโมลาร์" ด้วย "M" พร้อมกับสัญลักษณ์ทางเคมีตัวถูกละลาย
- ผลลัพธ์: 0.11 M NaCl