ผู้เขียน:
Eric Farmer
วันที่สร้าง:
10 มีนาคม 2021
วันที่อัปเดต:
1 กรกฎาคม 2024

เนื้อหา
- ขั้นตอน
- วิธีที่ 1 จาก 2: การกำหนดจำนวนนิวตรอนในอะตอม (ไม่ใช่ไอโซโทป)
- วิธีที่ 2 จาก 2: การหาจำนวนนิวตรอนในไอโซโทป
- เคล็ดลับ
ในอะตอมของธาตุเดียวกัน จำนวนโปรตอนจะคงที่ ในขณะที่จำนวนนิวตรอนอาจแตกต่างกันไปเมื่อทราบจำนวนนิวตรอนในอะตอม คุณจะสามารถระบุได้ว่าอะตอมนั้นเป็นอะตอมปกติหรือไอโซโทปที่จะมีนิวตรอนน้อยกว่าหรือมากกว่านั้น การหาจำนวนนิวตรอนในอะตอมนั้นค่อนข้างง่าย สิ่งที่คุณต้องทำเพื่อคำนวณจำนวนนิวตรอนในอะตอมหรือไอโซโทปคือการปฏิบัติตามคำแนะนำของเราและทำให้ตารางธาตุมีประโยชน์
ขั้นตอน
วิธีที่ 1 จาก 2: การกำหนดจำนวนนิวตรอนในอะตอม (ไม่ใช่ไอโซโทป)
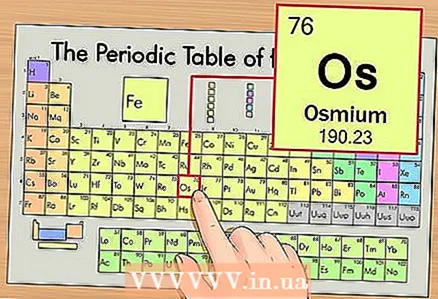 1 หาธาตุในตารางธาตุ. ตัวอย่างเช่น เราจะพิจารณาออสเมียม (Os) ซึ่งอยู่ในช่วงที่หก (แถวที่หกจากด้านบน)
1 หาธาตุในตารางธาตุ. ตัวอย่างเช่น เราจะพิจารณาออสเมียม (Os) ซึ่งอยู่ในช่วงที่หก (แถวที่หกจากด้านบน)  2 หาเลขอะตอมของธาตุ. ตามกฎแล้ว เป็นตัวเลขที่เห็นได้ชัดเจนที่สุดในเซลล์ขององค์ประกอบและมักจะอยู่เหนือสัญลักษณ์ (ในเวอร์ชันของตารางธาตุที่เราใช้ในตัวอย่าง ไม่มีตัวเลขอื่น) เลขอะตอมคือจำนวนโปรตอนในหนึ่งอะตอมของธาตุนั้น สำหรับออสเมียม ตัวเลขนี้คือ 76 นั่นคือมี 76 โปรตอนในหนึ่งอะตอมของออสเมียม
2 หาเลขอะตอมของธาตุ. ตามกฎแล้ว เป็นตัวเลขที่เห็นได้ชัดเจนที่สุดในเซลล์ขององค์ประกอบและมักจะอยู่เหนือสัญลักษณ์ (ในเวอร์ชันของตารางธาตุที่เราใช้ในตัวอย่าง ไม่มีตัวเลขอื่น) เลขอะตอมคือจำนวนโปรตอนในหนึ่งอะตอมของธาตุนั้น สำหรับออสเมียม ตัวเลขนี้คือ 76 นั่นคือมี 76 โปรตอนในหนึ่งอะตอมของออสเมียม - จำนวนโปรตอนไม่เปลี่ยนแปลง และนี่คือสิ่งที่ทำให้องค์ประกอบเป็นองค์ประกอบ
 3 หามวลอะตอมของธาตุ. ตัวเลขนี้มักจะอยู่ใต้สัญลักษณ์องค์ประกอบ โปรดทราบว่าในเวอร์ชันของตารางธาตุในตัวอย่างของเรา จะไม่มีการระบุมวลอะตอม (ซึ่งไม่ได้เป็นเช่นนั้นเสมอไป ในตารางธาตุหลายรุ่น มวลอะตอมจะถูกระบุ) มวลอะตอมของออสเมียมคือ 190.23
3 หามวลอะตอมของธาตุ. ตัวเลขนี้มักจะอยู่ใต้สัญลักษณ์องค์ประกอบ โปรดทราบว่าในเวอร์ชันของตารางธาตุในตัวอย่างของเรา จะไม่มีการระบุมวลอะตอม (ซึ่งไม่ได้เป็นเช่นนั้นเสมอไป ในตารางธาตุหลายรุ่น มวลอะตอมจะถูกระบุ) มวลอะตอมของออสเมียมคือ 190.23  4 ปัดเศษมวลอะตอมเป็นจำนวนเต็มที่ใกล้ที่สุด ในตัวอย่างของเรา 190.23 ถูกปัดเศษเป็น 190
4 ปัดเศษมวลอะตอมเป็นจำนวนเต็มที่ใกล้ที่สุด ในตัวอย่างของเรา 190.23 ถูกปัดเศษเป็น 190 - มวลอะตอมคือจำนวนไอโซโทปเฉลี่ยของธาตุใดธาตุหนึ่ง โดยปกติจะไม่แสดงเป็นจำนวนเต็ม
 5 ลบเลขอะตอมออกจากมวลอะตอม เนื่องจากโปรตอนและนิวตรอนคิดเป็นสัดส่วนสัมบูรณ์ของมวลอะตอม การลบจำนวนโปรตอน (นั่นคือ เลขอะตอม ซึ่งเท่ากับจำนวนโปรตอน) ออกจากมวลอะตอมจะทำให้จำนวนนิวตรอนในอะตอม ตัวเลขหลังจุดทศนิยมหมายถึงมวลอิเล็กตรอนที่น้อยมากในอะตอม ในตัวอย่างของเรา: 190 (น้ำหนักอะตอม) - 76 (จำนวนโปรตอน) = 114 (จำนวนนิวตรอน)
5 ลบเลขอะตอมออกจากมวลอะตอม เนื่องจากโปรตอนและนิวตรอนคิดเป็นสัดส่วนสัมบูรณ์ของมวลอะตอม การลบจำนวนโปรตอน (นั่นคือ เลขอะตอม ซึ่งเท่ากับจำนวนโปรตอน) ออกจากมวลอะตอมจะทำให้จำนวนนิวตรอนในอะตอม ตัวเลขหลังจุดทศนิยมหมายถึงมวลอิเล็กตรอนที่น้อยมากในอะตอม ในตัวอย่างของเรา: 190 (น้ำหนักอะตอม) - 76 (จำนวนโปรตอน) = 114 (จำนวนนิวตรอน) 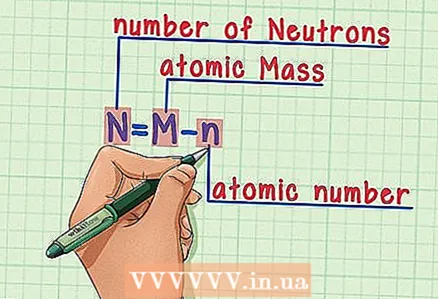 6 จำสูตร. ในการหาจำนวนนิวตรอนในอนาคต เพียงแค่ใช้สูตรนี้:
6 จำสูตร. ในการหาจำนวนนิวตรอนในอนาคต เพียงแค่ใช้สูตรนี้: - N = M - n
- N = จำนวนนิวตรอน
- M = มวลอะตอม
- n = เลขอะตอม
- N = M - n
วิธีที่ 2 จาก 2: การหาจำนวนนิวตรอนในไอโซโทป
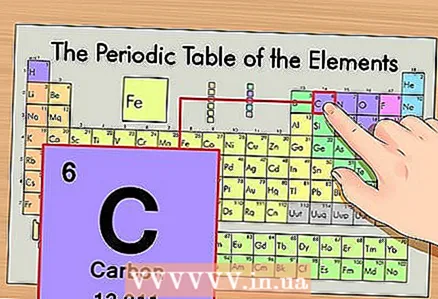 1 หาธาตุในตารางธาตุ. ตัวอย่างเช่น เราจะพิจารณาไอโซโทปของคาร์บอน 14C เนื่องจากคาร์บอนที่ไม่ใช่ไอโซโทป 14C เป็นเพียงคาร์บอน C ให้หาคาร์บอนในตารางธาตุ (ช่วงที่สองหรือแถวที่สองจากด้านบน)
1 หาธาตุในตารางธาตุ. ตัวอย่างเช่น เราจะพิจารณาไอโซโทปของคาร์บอน 14C เนื่องจากคาร์บอนที่ไม่ใช่ไอโซโทป 14C เป็นเพียงคาร์บอน C ให้หาคาร์บอนในตารางธาตุ (ช่วงที่สองหรือแถวที่สองจากด้านบน) 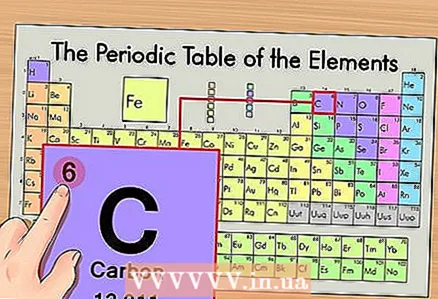 2 หาเลขอะตอมของธาตุ. ตามกฎแล้ว เป็นตัวเลขที่เห็นได้ชัดเจนที่สุดในเซลล์ขององค์ประกอบและมักจะอยู่เหนือสัญลักษณ์ (ในเวอร์ชันของตารางธาตุที่เราใช้ในตัวอย่าง ไม่มีตัวเลขอื่น) เลขอะตอมคือจำนวนโปรตอนในหนึ่งอะตอมของธาตุนั้น คาร์บอนเป็นเลข 6 ซึ่งหมายความว่าคาร์บอนหนึ่งตัวมีหกโปรตอน
2 หาเลขอะตอมของธาตุ. ตามกฎแล้ว เป็นตัวเลขที่เห็นได้ชัดเจนที่สุดในเซลล์ขององค์ประกอบและมักจะอยู่เหนือสัญลักษณ์ (ในเวอร์ชันของตารางธาตุที่เราใช้ในตัวอย่าง ไม่มีตัวเลขอื่น) เลขอะตอมคือจำนวนโปรตอนในหนึ่งอะตอมของธาตุนั้น คาร์บอนเป็นเลข 6 ซึ่งหมายความว่าคาร์บอนหนึ่งตัวมีหกโปรตอน 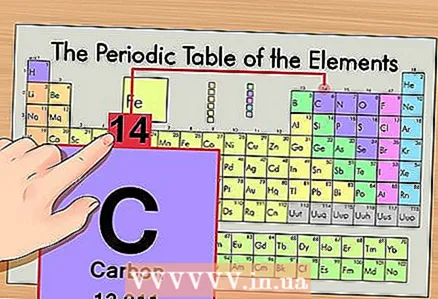 3 หามวลอะตอม. ในกรณีของไอโซโทป ทำได้ง่ายมาก เนื่องจากตั้งชื่อตามมวลอะตอมของพวกมัน ในกรณีของเรา คาร์บอน 14C มีมวลอะตอมเท่ากับ 14 ตอนนี้เรารู้มวลอะตอมของไอโซโทปแล้ว กระบวนการคำนวณที่ตามมาจะเหมือนกับการกำหนดจำนวนนิวตรอนในอะตอม (ไม่ใช่ไอโซโทป)
3 หามวลอะตอม. ในกรณีของไอโซโทป ทำได้ง่ายมาก เนื่องจากตั้งชื่อตามมวลอะตอมของพวกมัน ในกรณีของเรา คาร์บอน 14C มีมวลอะตอมเท่ากับ 14 ตอนนี้เรารู้มวลอะตอมของไอโซโทปแล้ว กระบวนการคำนวณที่ตามมาจะเหมือนกับการกำหนดจำนวนนิวตรอนในอะตอม (ไม่ใช่ไอโซโทป)  4 ลบเลขอะตอมออกจากมวลอะตอม เนื่องจากโปรตอนและนิวตรอนคิดเป็นสัดส่วนสัมบูรณ์ของมวลอะตอม การลบจำนวนโปรตอน (นั่นคือ เลขอะตอม ซึ่งเท่ากับจำนวนโปรตอน) ออกจากมวลอะตอมจะทำให้จำนวนนิวตรอนในอะตอม ในตัวอย่างของเรา: 14 (มวลอะตอม) - 6 (จำนวนโปรตอน) = 8 (จำนวนนิวตรอน)
4 ลบเลขอะตอมออกจากมวลอะตอม เนื่องจากโปรตอนและนิวตรอนคิดเป็นสัดส่วนสัมบูรณ์ของมวลอะตอม การลบจำนวนโปรตอน (นั่นคือ เลขอะตอม ซึ่งเท่ากับจำนวนโปรตอน) ออกจากมวลอะตอมจะทำให้จำนวนนิวตรอนในอะตอม ในตัวอย่างของเรา: 14 (มวลอะตอม) - 6 (จำนวนโปรตอน) = 8 (จำนวนนิวตรอน) 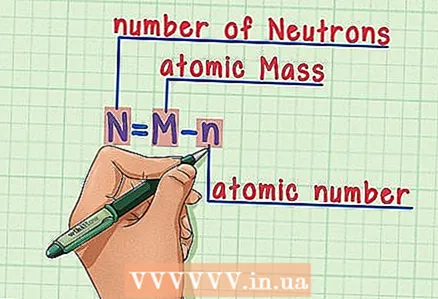 5 จำสูตร. ในการหาจำนวนนิวตรอนในอนาคต เพียงแค่ใช้สูตรนี้:
5 จำสูตร. ในการหาจำนวนนิวตรอนในอนาคต เพียงแค่ใช้สูตรนี้: - N = M - n
- N = จำนวนนิวตรอน
- M = มวลอะตอม
- n = เลขอะตอม
- N = M - n
เคล็ดลับ
- โปรตอนและนิวตรอนประกอบขึ้นเป็นมวลสัมบูรณ์ของธาตุ ขณะที่อิเล็กตรอนและอนุภาคอื่นๆ รวมกันเป็นมวลที่ไม่มีนัยสำคัญอย่างยิ่ง (มวลนี้มีแนวโน้มเป็นศูนย์)เนื่องจากโปรตอนหนึ่งตัวมีมวลเท่ากับหนึ่งนิวตรอน และเลขอะตอมคือจำนวนโปรตอน คุณจึงสามารถลบจำนวนโปรตอนออกจากมวลรวมได้
- Osmium - โลหะในสถานะของแข็งที่อุณหภูมิห้องได้ชื่อมาจากคำภาษากรีก "osme" - กลิ่น
- หากคุณไม่แน่ใจว่าตัวเลขในตารางธาตุหมายถึงอะไร โปรดจำไว้ว่า: ตารางมักจะสร้างจากเลขอะตอม (นั่นคือจำนวนโปรตอน) ซึ่งเริ่มต้นที่ 1 (ไฮโดรเจน) และเพิ่มขึ้นหนึ่งหน่วยจากซ้ายไปขวา , ลงท้ายด้วย 118 (โอกาเนสสัน). เนื่องจากจำนวนโปรตอนในอะตอมเป็นตัวกำหนดองค์ประกอบ และจำนวนดังกล่าวเป็นวิธีที่ง่ายที่สุดในการจัดระเบียบองค์ประกอบ (เช่น อะตอมที่มี 2 โปรตอนจะเป็นฮีเลียมเสมอ เช่นเดียวกับอะตอมที่มีโปรตอน 79 ตัวจะเป็นสีทองเสมอ ).