ผู้เขียน:
Sara Rhodes
วันที่สร้าง:
12 กุมภาพันธ์ 2021
วันที่อัปเดต:
1 กรกฎาคม 2024
![🧪เลขออกซิเดชัน [Chemistry#38]](https://i.ytimg.com/vi/OFdBrcC61C4/hqdefault.jpg)
เนื้อหา
- ขั้นตอน
- ส่วนที่ 1 จาก 2: การหาสถานะออกซิเดชันตามกฎเคมี
- ส่วนที่ 2 ของ 2: การหาสถานะออกซิเดชันโดยไม่ต้องใช้กฎเคมี
- เคล็ดลับ
- อะไรที่คุณต้องการ
ในทางเคมี คำว่า "ออกซิเดชัน" และ "รีดักชัน" หมายถึงปฏิกิริยาที่อะตอมหรือกลุ่มของอะตอมสูญเสียหรือได้รับอิเล็กตรอนตามลำดับ สถานะออกซิเดชันเป็นค่าตัวเลขที่กำหนดให้กับอะตอมตั้งแต่หนึ่งอะตอมขึ้นไปซึ่งระบุลักษณะเฉพาะของจำนวนอิเล็กตรอนที่กระจายตัวและแสดงให้เห็นว่าอิเล็กตรอนเหล่านี้ถูกกระจายระหว่างอะตอมระหว่างปฏิกิริยาอย่างไร การหาค่านี้สามารถเป็นขั้นตอนที่ง่ายและค่อนข้างซับซ้อน ขึ้นอยู่กับอะตอมและโมเลกุลที่ประกอบด้วยพวกมัน นอกจากนี้ อะตอมของธาตุบางชนิดสามารถมีสถานะออกซิเดชันได้หลายสถานะ โชคดีที่มีกฎเกณฑ์ง่ายๆ ที่ชัดเจนในการกำหนดสถานะออกซิเดชัน สำหรับการใช้อย่างมั่นใจซึ่งเพียงพอที่จะรู้พื้นฐานของเคมีและพีชคณิต
ขั้นตอน
ส่วนที่ 1 จาก 2: การหาสถานะออกซิเดชันตามกฎเคมี
 1 พิจารณาว่าสารที่เป็นปัญหานั้นเป็นธาตุหรือไม่. สถานะออกซิเดชันของอะตอมที่อยู่นอกสารประกอบเคมีเป็นศูนย์ กฎนี้เป็นจริงทั้งสำหรับสารที่เกิดขึ้นจากอะตอมอิสระที่แยกจากกัน และสำหรับสารที่ประกอบด้วยสองหรือโมเลกุลหลายอะตอมขององค์ประกอบเดียว
1 พิจารณาว่าสารที่เป็นปัญหานั้นเป็นธาตุหรือไม่. สถานะออกซิเดชันของอะตอมที่อยู่นอกสารประกอบเคมีเป็นศูนย์ กฎนี้เป็นจริงทั้งสำหรับสารที่เกิดขึ้นจากอะตอมอิสระที่แยกจากกัน และสำหรับสารที่ประกอบด้วยสองหรือโมเลกุลหลายอะตอมขององค์ประกอบเดียว - ตัวอย่างเช่น Al(NS) และ Cl2 มีสถานะออกซิเดชันเป็น 0 เนื่องจากทั้งสองอยู่ในสถานะองค์ประกอบที่ไม่ผูกมัดทางเคมี
- โปรดทราบว่ารูปแบบ allotropic ของกำมะถัน S8หรือ octacera แม้จะมีโครงสร้างผิดปกติ แต่ก็มีลักษณะเป็นศูนย์ออกซิเดชัน
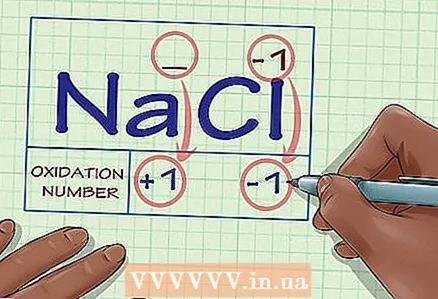 2 ตรวจสอบว่าสารที่เป็นปัญหาประกอบด้วยไอออนหรือไม่ สถานะออกซิเดชันของไอออนเท่ากับประจุ สิ่งนี้เป็นจริงทั้งสำหรับไอออนอิสระและสำหรับไอออนที่เป็นส่วนหนึ่งของสารประกอบทางเคมี
2 ตรวจสอบว่าสารที่เป็นปัญหาประกอบด้วยไอออนหรือไม่ สถานะออกซิเดชันของไอออนเท่ากับประจุ สิ่งนี้เป็นจริงทั้งสำหรับไอออนอิสระและสำหรับไอออนที่เป็นส่วนหนึ่งของสารประกอบทางเคมี - ตัวอย่างเช่น สถานะออกซิเดชันของไอออน Cl คือ -1
- สถานะออกซิเดชันของไอออน Cl ในสารประกอบทางเคมี NaCl ก็คือ -1 ด้วย เนื่องจาก Na ion ตามคำจำกัดความมีประจุ +1 เราจึงสรุปได้ว่าประจุของ Cl ion คือ -1 ดังนั้นสถานะออกซิเดชันของมันคือ -1
 3 โปรดทราบว่าไอออนของโลหะสามารถมีสถานะออกซิเดชันได้หลายสถานะ อะตอมของธาตุโลหะหลายชนิดสามารถแตกตัวเป็นไอออนได้ในปริมาณที่แตกต่างกัน ตัวอย่างเช่น ประจุไอออนของโลหะ เช่น เหล็ก (Fe) คือ +2 หรือ +3 ประจุของไอออนของโลหะ (และสถานะออกซิเดชันของพวกมัน) สามารถกำหนดได้โดยประจุของไอออนของธาตุอื่นๆ ที่โลหะนี้เป็นส่วนหนึ่งของสารประกอบทางเคมี ในข้อความ ประจุนี้แสดงด้วยเลขโรมัน ตัวอย่างเช่น เหล็ก (III) มีสถานะออกซิเดชันเป็น +3
3 โปรดทราบว่าไอออนของโลหะสามารถมีสถานะออกซิเดชันได้หลายสถานะ อะตอมของธาตุโลหะหลายชนิดสามารถแตกตัวเป็นไอออนได้ในปริมาณที่แตกต่างกัน ตัวอย่างเช่น ประจุไอออนของโลหะ เช่น เหล็ก (Fe) คือ +2 หรือ +3 ประจุของไอออนของโลหะ (และสถานะออกซิเดชันของพวกมัน) สามารถกำหนดได้โดยประจุของไอออนของธาตุอื่นๆ ที่โลหะนี้เป็นส่วนหนึ่งของสารประกอบทางเคมี ในข้อความ ประจุนี้แสดงด้วยเลขโรมัน ตัวอย่างเช่น เหล็ก (III) มีสถานะออกซิเดชันเป็น +3 - ตัวอย่างเช่น ให้พิจารณาสารประกอบที่มีอะลูมิเนียมไอออน ค่าใช้จ่ายทั้งหมดของสารประกอบ AlCl3 เป็นศูนย์เนื่องจากเรารู้ว่าไอออนของ Cl มีประจุเป็น -1 และสารประกอบนั้นมีไอออนดังกล่าว 3 ตัว สำหรับความเป็นกลางทั่วไปของสารที่เป็นปัญหา ไอออน Al ต้องมีประจุเป็น +3 ดังนั้น ในกรณีนี้ สถานะออกซิเดชันของอะลูมิเนียมคือ +3
 4 สถานะออกซิเดชันของออกซิเจนคือ -2 (มีข้อยกเว้นบางประการ) ในเกือบทุกกรณี อะตอมของออกซิเจนมีสถานะออกซิเดชันเป็น -2 มีข้อยกเว้นหลายประการสำหรับกฎนี้:
4 สถานะออกซิเดชันของออกซิเจนคือ -2 (มีข้อยกเว้นบางประการ) ในเกือบทุกกรณี อะตอมของออกซิเจนมีสถานะออกซิเดชันเป็น -2 มีข้อยกเว้นหลายประการสำหรับกฎนี้: - ถ้าออกซิเจนอยู่ในสถานะธาตุ (O2) สถานะออกซิเดชันของมันคือ 0 เช่นเดียวกับในกรณีของสารพื้นฐานอื่นๆ
- ถ้าออกซิเจนเป็นส่วนหนึ่งของ เปอร์ออกไซด์สถานะออกซิเดชันของมันคือ -1 เปอร์ออกไซด์เป็นกลุ่มของสารประกอบที่มีพันธะออกซิเจนกับออกซิเจนอย่างง่าย (เช่น แอนไอออนของเปอร์ออกไซด์ O2). ตัวอย่างเช่น ในองค์ประกอบของH2อู๋2 (ไฮโดรเจนเปอร์ออกไซด์) ออกซิเจนมีประจุและสถานะออกซิเดชันเป็น -1
- เมื่อรวมกับฟลูออรีน ออกซิเจนจะมีสถานะออกซิเดชันเท่ากับ +2 อ่านกฎของฟลูออรีนด้านล่าง
 5 ไฮโดรเจนมีสถานะออกซิเดชันเป็น +1 โดยมีข้อยกเว้นบางประการ เช่นเดียวกับออกซิเจนก็มีข้อยกเว้นเช่นกัน ตามกฎแล้วสถานะออกซิเดชันของไฮโดรเจนคือ +1 (หากไม่ได้อยู่ในสถานะธาตุH2). อย่างไรก็ตาม ในสารประกอบที่เรียกว่าไฮไดรด์ สถานะออกซิเดชันของไฮโดรเจนคือ -1
5 ไฮโดรเจนมีสถานะออกซิเดชันเป็น +1 โดยมีข้อยกเว้นบางประการ เช่นเดียวกับออกซิเจนก็มีข้อยกเว้นเช่นกัน ตามกฎแล้วสถานะออกซิเดชันของไฮโดรเจนคือ +1 (หากไม่ได้อยู่ในสถานะธาตุH2). อย่างไรก็ตาม ในสารประกอบที่เรียกว่าไฮไดรด์ สถานะออกซิเดชันของไฮโดรเจนคือ -1 - ตัวอย่างเช่น ใน H2O สถานะออกซิเดชันของไฮโดรเจนคือ +1 เนื่องจากอะตอมของออกซิเจนมีประจุเป็น -2 และจำเป็นต้องมีประจุ +1 สองประจุสำหรับความเป็นกลางโดยรวม อย่างไรก็ตาม ในองค์ประกอบของโซเดียมไฮไดรด์ สถานะออกซิเดชันของไฮโดรเจนมีอยู่แล้ว -1 เนื่องจากไอออน Na มีประจุ +1 และสำหรับอิเล็กโตรนิวตริลิตีทั่วไป ประจุของอะตอมไฮโดรเจน (และด้วยเหตุนี้สถานะออกซิเดชัน) จึงควร เป็น -1
 6 ฟลูออรีน เสมอ มีสถานะออกซิเดชันเป็น -1 ตามที่ระบุไว้แล้ว สถานะออกซิเดชันของธาตุบางชนิด (ไอออนของโลหะ อะตอมของออกซิเจนในเปอร์ออกไซด์ เป็นต้น) อาจแตกต่างกันไปขึ้นอยู่กับปัจจัยหลายประการ อย่างไรก็ตาม สถานะออกซิเดชันของฟลูออรีนมีค่าเท่ากับ -1 อย่างสม่ำเสมอ เนื่องจากองค์ประกอบนี้มีอิเล็กโตรเนกาติวีตี้มากที่สุด กล่าวคือ อะตอมของฟลูออรีนมีความเต็มใจน้อยที่สุดที่จะมีส่วนร่วมกับอิเล็กตรอนของพวกมันเอง และดึงดูดอิเล็กตรอนจากต่างประเทศอย่างแข็งขันที่สุด ดังนั้นค่าใช้จ่ายของพวกเขายังคงไม่เปลี่ยนแปลง
6 ฟลูออรีน เสมอ มีสถานะออกซิเดชันเป็น -1 ตามที่ระบุไว้แล้ว สถานะออกซิเดชันของธาตุบางชนิด (ไอออนของโลหะ อะตอมของออกซิเจนในเปอร์ออกไซด์ เป็นต้น) อาจแตกต่างกันไปขึ้นอยู่กับปัจจัยหลายประการ อย่างไรก็ตาม สถานะออกซิเดชันของฟลูออรีนมีค่าเท่ากับ -1 อย่างสม่ำเสมอ เนื่องจากองค์ประกอบนี้มีอิเล็กโตรเนกาติวีตี้มากที่สุด กล่าวคือ อะตอมของฟลูออรีนมีความเต็มใจน้อยที่สุดที่จะมีส่วนร่วมกับอิเล็กตรอนของพวกมันเอง และดึงดูดอิเล็กตรอนจากต่างประเทศอย่างแข็งขันที่สุด ดังนั้นค่าใช้จ่ายของพวกเขายังคงไม่เปลี่ยนแปลง  7 ผลรวมของสถานะออกซิเดชันในสารประกอบเท่ากับประจุของมัน สถานะออกซิเดชันของอะตอมทั้งหมดที่ประกอบเป็นสารประกอบทางเคมีควรรวมกันเป็นประจุของสารประกอบนี้ ตัวอย่างเช่น หากสารประกอบเป็นกลาง ผลรวมของสถานะออกซิเดชันของอะตอมทั้งหมดควรเป็นศูนย์ ถ้าสารประกอบนั้นเป็นโพลีอะตอมมิกไอออนที่มีประจุ -1 ผลรวมของสถานะออกซิเดชันจะเท่ากับ -1 เป็นต้น
7 ผลรวมของสถานะออกซิเดชันในสารประกอบเท่ากับประจุของมัน สถานะออกซิเดชันของอะตอมทั้งหมดที่ประกอบเป็นสารประกอบทางเคมีควรรวมกันเป็นประจุของสารประกอบนี้ ตัวอย่างเช่น หากสารประกอบเป็นกลาง ผลรวมของสถานะออกซิเดชันของอะตอมทั้งหมดควรเป็นศูนย์ ถ้าสารประกอบนั้นเป็นโพลีอะตอมมิกไอออนที่มีประจุ -1 ผลรวมของสถานะออกซิเดชันจะเท่ากับ -1 เป็นต้น - นี่เป็นวิธีการทดสอบที่ดี ถ้าผลรวมของสถานะออกซิเดชันไม่เท่ากับประจุทั้งหมดของสารประกอบ แสดงว่าคุณคิดผิด
ส่วนที่ 2 ของ 2: การหาสถานะออกซิเดชันโดยไม่ต้องใช้กฎเคมี
 1 ค้นหาอะตอมที่ไม่มีกฎเกณฑ์ที่เข้มงวดเกี่ยวกับสถานะออกซิเดชัน สำหรับองค์ประกอบบางอย่าง ไม่มีกฎเกณฑ์ที่ชัดเจนในการค้นหาสถานะออกซิเดชัน หากอะตอมไม่เป็นไปตามกฎที่ระบุไว้ข้างต้น และคุณไม่ทราบประจุของอะตอม (เช่น อะตอมเป็นส่วนหนึ่งของคอมเพล็กซ์และไม่มีการระบุประจุ) คุณสามารถกำหนดสถานะออกซิเดชันของอะตอมดังกล่าวได้ โดยการยกเว้น ขั้นแรก หาประจุของอะตอมอื่นๆ ทั้งหมดในสารประกอบ จากนั้นคำนวณสถานะออกซิเดชันของอะตอมนี้จากประจุทั้งหมดที่ทราบของสารประกอบ
1 ค้นหาอะตอมที่ไม่มีกฎเกณฑ์ที่เข้มงวดเกี่ยวกับสถานะออกซิเดชัน สำหรับองค์ประกอบบางอย่าง ไม่มีกฎเกณฑ์ที่ชัดเจนในการค้นหาสถานะออกซิเดชัน หากอะตอมไม่เป็นไปตามกฎที่ระบุไว้ข้างต้น และคุณไม่ทราบประจุของอะตอม (เช่น อะตอมเป็นส่วนหนึ่งของคอมเพล็กซ์และไม่มีการระบุประจุ) คุณสามารถกำหนดสถานะออกซิเดชันของอะตอมดังกล่าวได้ โดยการยกเว้น ขั้นแรก หาประจุของอะตอมอื่นๆ ทั้งหมดในสารประกอบ จากนั้นคำนวณสถานะออกซิเดชันของอะตอมนี้จากประจุทั้งหมดที่ทราบของสารประกอบ - ตัวอย่างเช่น ในสารประกอบ Na2ดังนั้น4 ไม่ทราบประจุของอะตอมกำมะถัน (S) - เรารู้แค่ว่ามันไม่ใช่ศูนย์ เนื่องจากกำมะถันไม่อยู่ในสถานะพื้นฐาน สารประกอบนี้ทำหน้าที่เป็นตัวอย่างที่ดีในการแสดงวิธีพีชคณิตสำหรับการกำหนดสถานะออกซิเดชัน
 2 ค้นหาสถานะออกซิเดชันของธาตุที่เหลือในสารประกอบ ใช้กฎที่อธิบายไว้ข้างต้น กำหนดสถานะออกซิเดชันของอะตอมที่เหลืออยู่ของสารประกอบ อย่าลืมข้อยกเว้นของกฎสำหรับ O, H และอื่นๆ
2 ค้นหาสถานะออกซิเดชันของธาตุที่เหลือในสารประกอบ ใช้กฎที่อธิบายไว้ข้างต้น กำหนดสถานะออกซิเดชันของอะตอมที่เหลืออยู่ของสารประกอบ อย่าลืมข้อยกเว้นของกฎสำหรับ O, H และอื่นๆ - สำหรับ Na2ดังนั้น4เมื่อใช้กฎของเรา เราพบว่าประจุ (และด้วยเหตุนี้สถานะออกซิเดชัน) ของไอออน Na คือ +1 และสำหรับอะตอมออกซิเจนแต่ละอะตอม มันคือ -2
 3 คูณจำนวนอะตอมด้วยสถานะออกซิเดชัน ตอนนี้เราทราบสถานะออกซิเดชันของอะตอมทั้งหมดแล้ว ยกเว้นเพียงอะตอมเดียว จำเป็นต้องคำนึงว่าอาจมีอะตอมหลายธาตุของธาตุบางชนิด คูณจำนวนอะตอมของธาตุแต่ละธาตุ (ระบุไว้ในสูตรทางเคมีของสารประกอบโดยเป็นตัวห้อยตามสัญลักษณ์ของธาตุ) ด้วยสถานะออกซิเดชัน
3 คูณจำนวนอะตอมด้วยสถานะออกซิเดชัน ตอนนี้เราทราบสถานะออกซิเดชันของอะตอมทั้งหมดแล้ว ยกเว้นเพียงอะตอมเดียว จำเป็นต้องคำนึงว่าอาจมีอะตอมหลายธาตุของธาตุบางชนิด คูณจำนวนอะตอมของธาตุแต่ละธาตุ (ระบุไว้ในสูตรทางเคมีของสารประกอบโดยเป็นตัวห้อยตามสัญลักษณ์ของธาตุ) ด้วยสถานะออกซิเดชัน - ในนา2ดังนั้น4 เรามีอะตอม Na 2 ตัวและอะตอม O 4 ตัว ดังนั้น เมื่อคูณ 2 × +1 เราจะได้สถานะออกซิเดชันของอะตอม Na ทั้งหมด (2) และคูณ 4 × -2 - สถานะออกซิเดชันของอะตอม O (-8)
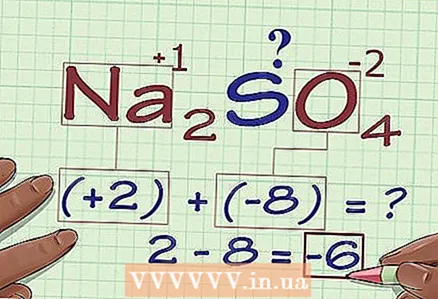 4 บวกผลลัพธ์ก่อนหน้า เมื่อสรุปผลลัพธ์ของการคูณ เราได้สถานะออกซิเดชันของสารประกอบ ปราศจาก โดยคำนึงถึงการมีส่วนร่วมของอะตอมที่ต้องการ
4 บวกผลลัพธ์ก่อนหน้า เมื่อสรุปผลลัพธ์ของการคูณ เราได้สถานะออกซิเดชันของสารประกอบ ปราศจาก โดยคำนึงถึงการมีส่วนร่วมของอะตอมที่ต้องการ - ในตัวอย่างของเรา สำหรับ Na2ดังนั้น4 เราบวก 2 และ -8 และรับ -6
 5 ค้นหาสถานะออกซิเดชันที่ไม่รู้จักจากประจุของสารประกอบ ตอนนี้คุณมีข้อมูลทั้งหมดเพื่อคำนวณสถานะออกซิเดชันที่ต้องการได้อย่างง่ายดาย เขียนสมการที่ด้านซ้ายซึ่งจะมีผลรวมของจำนวนที่ได้รับในขั้นตอนการคำนวณก่อนหน้าและสถานะออกซิเดชันที่ไม่รู้จัก และทางด้านขวาของประจุทั้งหมดของสารประกอบ กล่าวอีกนัยหนึ่ง (ผลรวมของสถานะออกซิเดชันที่ทราบ) + (สถานะออกซิเดชันที่ต้องการ) = (ประจุของสารประกอบ)
5 ค้นหาสถานะออกซิเดชันที่ไม่รู้จักจากประจุของสารประกอบ ตอนนี้คุณมีข้อมูลทั้งหมดเพื่อคำนวณสถานะออกซิเดชันที่ต้องการได้อย่างง่ายดาย เขียนสมการที่ด้านซ้ายซึ่งจะมีผลรวมของจำนวนที่ได้รับในขั้นตอนการคำนวณก่อนหน้าและสถานะออกซิเดชันที่ไม่รู้จัก และทางด้านขวาของประจุทั้งหมดของสารประกอบ กล่าวอีกนัยหนึ่ง (ผลรวมของสถานะออกซิเดชันที่ทราบ) + (สถานะออกซิเดชันที่ต้องการ) = (ประจุของสารประกอบ)- ในกรณีของเรา Na2ดังนั้น4 วิธีแก้ปัญหามีลักษณะดังนี้:
- (ผลรวมของสถานะออกซิเดชันที่ทราบ) + (สถานะออกซิเดชันที่ต้องการ) = (ประจุผสม)
- -6 + S = 0
- S = 0 + 6
- S = 6.V Na2ดังนั้น4 กำมะถันมีสถานะออกซิเดชัน 6.
- ในกรณีของเรา Na2ดังนั้น4 วิธีแก้ปัญหามีลักษณะดังนี้:
เคล็ดลับ
- ในสารประกอบ ผลรวมของสถานะออกซิเดชันทั้งหมดต้องเท่ากับประจุ ตัวอย่างเช่น ถ้าสารประกอบเป็นไดอะตอมมิกไอออน ผลรวมของสถานะออกซิเดชันของอะตอมจะต้องเท่ากับประจุไอออนิกทั้งหมด
- มีประโยชน์มากที่จะสามารถใช้ตารางธาตุและรู้ว่าธาตุโลหะและอโลหะอยู่ตรงไหน
- สถานะออกซิเดชันของอะตอมในรูปแบบพื้นฐานจะเป็นศูนย์เสมอ สถานะออกซิเดชันของไอออนเดี่ยวมีค่าเท่ากับประจุของมัน องค์ประกอบของกลุ่ม 1A ของตารางธาตุ เช่น ไฮโดรเจน ลิเธียม โซเดียม ในรูปแบบธาตุมีสถานะออกซิเดชัน +1 สถานะออกซิเดชันของโลหะกลุ่ม 2A เช่น แมกนีเซียมและแคลเซียม คือ +2 ในรูปแบบธาตุ ออกซิเจนและไฮโดรเจน ขึ้นอยู่กับชนิดของพันธะเคมี สามารถมีสถานะออกซิเดชันได้ 2 สถานะ
อะไรที่คุณต้องการ
- ตารางธาตุ
- หนังสืออ้างอิงเกี่ยวกับอินเทอร์เน็ตหรือเคมี
- แผ่นกระดาษ ปากกา หรือดินสอ
- เครื่องคิดเลข



